

光源に高精度LEDを採用It uses a high-precision LED as the light source

発光効率がよく全光束が多い高精度LEDは、応答性に優れ、いかなる環境でも効果が安定します。振動や衝撃に強く、紫外線がほとんど出ない安全性も保持します。
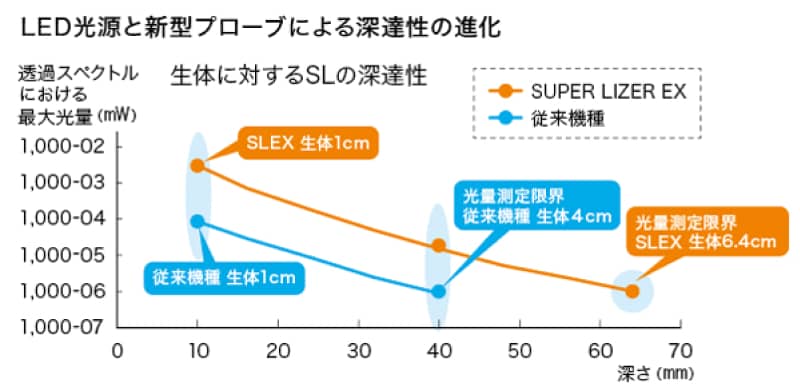
新たに開発されたLEDプローブでは、生体内で受け取る受光量を従来機の約5倍にすることを可能としました。
新波長帯を新たに採用Adoption of new wavelength band
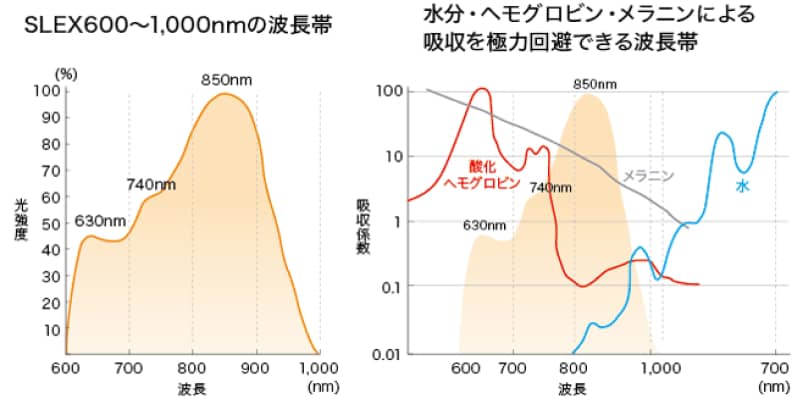
新たに600nm~1000nmの波長帯を採用しました。1000nm以上の波長帯をカットし、純粋に生体深達性に優れる波長帯のみを照射できます。
この波長帯とLED光源とのマッチングにより火傷の危険性を回避しつつ体内到達エネルギー量が大幅に増加させることに成功しました。
新開発 LED光源内蔵軽量プローブNewly developed lightweight probe with built-in LED light source
新たに開発したプローブは全て単体で光源を持ちます。
従来の光伝達ファイバーがなくなり超軽量化仕様になりました。
各プローブは症例、部位ごとに専用設計されており、それぞれ最適の照射面、光量にて照射できます。
生体深達度と深達光量は従来機より大幅に増加しています。
よくある質問がん光免疫療法に関する
FAQ
- どんな状態でも治療が受けられますか?
- 当院の治療は外来通院になります。無理なく来院できる患者様であれば、治療を受けていただく事が可能です。一部のがん種を除き、ほぼ全てのがん種、ステージ㈵期〜㈿期まで治療が可能です。詳しくは無料電話相談にてご相談下さい。
- がん光免疫療法に使用する機器は従来と何が違うのですか?
- 当院でがん光免疫療法に使用する機器は約30,000台の導入実績があり、およそ四半世紀の歴史を持つ東京医研株式会社の最新機器スーパーライザーEXです。スーパーライザーは光の中で最も生体深達性の高い波長帯の近赤外線を、高出力でスポット状に照射することを可能にした日本初の光線治療器です。パルス照射と呼ばれる照射方法で深達度を従来の機器に比べ格段にアップさせたものになります。
- 副作用が少ないのはなぜですか?
- がん光免疫療法で使用する薬剤は、正常細胞にダメージを与えるものではありません。また、治療時に照射するレーザー自体は手をかざしても熱さを感じないくらいの低エネルギーで、レーザー光の照射により人体に影響及ぼす心配はほぼありません。レーザー光の照射によって反応するのは薬剤が集積したがん細胞のみなので、がん細胞のみ破壊し、正常細胞は影響を受けないという事になります。
- 遠方からも通院する事は可能ですか?
- 当院で治療を受けられる患者様には遠方(他県)からの患者様も多くいらっしゃいますのでご安心下さい。当院では遠方の患者様も安心してご来院いただけるようサポートさせていただきます。詳しくは、医療コーディネーターまでご相談下さい。
- 紹介状や資料を持参する必要はありますか?
- 当院では、血液検査により治療効果を確認しつつ治療を行いますので医療記録の開示を必須とはしていません。しかし、これまでの血液検査結果、画像データ、遺伝子検査結果などお手持ちの情報がありましたらお持ち頂きたいと思います。
- まずは詳しい話を聞いてみたいのですが。
- 当院では、患者様とご家族様がご負担なくご相談いただける無料相談専用のフリーダイヤルをご用意しております。治療をご検討中の方や、治療についてご質問があれば、些細な事でも遠慮なくご相談下さい。ご自身の状態に合わせた治療についてより詳しくお知りになりたい方は医師による個別医療相談も行っています(事前予約制)。
スーパーライザーEXを用いたがん光免疫療法について
- がん光免疫療法は、国内未承認医薬品または医療機器を用いた施術が含まれます。公的医療保険は適用されません。
- がん光免疫療法は通常1クール計5回の通院治療を基本としていますが、患者様の状態により1クールで終了または2クール以降も継続する場合があります。
(2クール目以降も1クール2,200,000円(税込))1クールの治療を受けられた場合の標準的な費用は2,200,000円で治療期間はおよそ1ヵ月です。 - ICGリポソーム及びタラポルフィンリポソームは、合同会社革新的融合研究所にステルス化されたリポソームの製造を委託し、最終調合を院内で行っています。
- がん光免疫療法で用いられるICGリポソーム及びタラポルフィンリポソームは、日本国内に同一成分や性能を有する承認薬はありません。
- 光線力学的療法(Photodynamic Therapy:PDT)として国内にて承認済の医薬品等として以下のものがあります。
ルフィマーナトリウム:早期肺がん、早期食道がん、胃がん、早期子宮頚がんに対して、1994年に保険承認。 タラポルフィンナトリウム:早期肺癌、原発性悪性脳腫瘍、化学放射線療法又は放射線療法後の局所遺残再発食道癌に対して、2003年に保険承認。 セツキシマブサロタロカンナトリウム:切除不能な局所進行又は局所再発の頭頸部癌に対して、2020年に条件付早期承認。 - がん光免疫療法は、低侵襲性の副作用が少ない治療法ですが、稀に以下のような副作用が生じる場合があります。
アレルギー反応やアナフィラキシーショックが極稀(0.3%)に起こることがありますが、事前にアレルギー反応テストを行ない安全を確保した上で治療を開始します。 点滴の際に皮下血腫、神経損傷など合併症が起きることがあります。(一般的な採血・注射・点滴同様) 日焼けの可能性があります(1週間前後)。
